Тайская Эмульсия Flying Rabbit Abdominal Pain Flatulence Diarrhea Инструкция По Применению
Эмульсия Летающий белый кролик – это эффективное и быстрое средство от отравлений, от боли и спазмов в животе, от диареи, тошноты и рвоты. Эмульсия Flying Rabbit известна в Таиланде уже более 70 лет, это настоящая скорая помощь при отравлениях и неприятных ощущениях в животе.
Тайское средство Летающий кролик практически за 20 минут снимает неприятные и болезненные ощущения в животе, спазмы, колики, тошноту и сразу же останавливает диарею.
Эмульсия имеет приятный мятный вкус.
Активные вещества в составе эмульсии, в 100 мл.
- Салол 2 гр. – антисептическое, жаропонижающее и противовоспалительное действие;
- Анисовое масло 0,132 мл. – снимает спазмы в кишечнике, устраняет боль в животе, способствует пищеварению, ускоряет перистальтику и устраняет газообразование;
- Ментол 0,176 гр. – общий антисептик, улучшает работу желудка, снимает тошноту, обладает противоспазматическим и глистогонным действием.
Показания к применению
- пищевые и алкогольных отравленя;
- боли в желудке и кишечнике;
- при диарее, тошноте, рвоте и изжоге;
- при энтероколите и колите.
Способ применения
Перед применением бутылочку с эмульсией взболтать.
Взрослым
- 1 столовая ложка
Детям
- 1-2 чайные ложки
Средство Flying Rabbit abdominal pain не требует запивания.
Через 20 минут при необходимости можно повторить прием препарата.
Способ хранения
Хранить при комнатной температуре, в темном месте, не доступным детям.
Противопоказания
Индивидуальная непереносимость.
Объем: 50/200 мл. на Ваш выбор
Препарат сертифицирован и продается в аптеках Таиланда без рецепта. Перед применением требуется консультация специалиста.
Тайская Эмульсия Flying Rabbit Abdominal Pain Flatulence Diarrhea Инструкция По Применению
Эмульсия Летающий белый кролик – это эффективное и быстрое средство от отравлений, от боли и спазмов в животе, от диареи, тошноты и рвоты. Эмульсия Flying Rabbit известна в Таиланде уже более 70 лет, это настоящая скорая помощь при отравлениях и неприятных ощущениях в животе.
Показания к применению
- пищевые и алкогольных отравления;
- боли в желудке и кишечнике;
- при диарее, тошноте, рвоте и изжоге;
- при энтероколите и колите.
Эффект от применения
Тайское средство Летающий кролик за 20 минут снимает неприятные и болезненные ощущения в животе, спазмы, колики, тошноту и сразу же останавливает диарею.
Эмульсия имеет приятный мятный вкус.
Активные вещества в составе эмульсии, в 100 мл.
- Салол 2 гр. – антисептическое, жаропонижающее и противовоспалительное действие;
- Анисовое масло 0,132 мл. – снимает спазмы в кишечнике, устраняет боль в животе, способствует пищеварению, ускоряет перистальтику и устраняет газообразование;
- Ментол 0,176 гр. – общий антисептик, улучшает работу желудка, снимает тошноту, обладает противоспазматическим и глистогонным действием.
Способ применения
Перед применением бутылочку с эмульсией взболтать.
Взрослым
- 1 столовая ложка
Детям
- 1-2 чайные ложки
Средство Flying Rabbit abdominal pain не требует запивания.
Через 20 минут при необходимости можно повторить прием препарата.
Противопоказания
Индивидуальная непереносимость
Побочные действия
При соблюдении рекомендованной дозы отсутствуют
Особые указания
Хранить в местах, недоступных детям
Избегать передозировки
Способ хранения
Хранить в сухом прохладном месте
Беречь от попадания прямого солнечного света
Состав
Салол – 2 гр., Анисовое масло – 0,132 мл., Ментол – 0,176 гр.
Срок годности
Указан производителем на упаковке
Объем: 50/200 мл. на Ваш выбор
Производство: Flying Rabbit, Таиланд
Пищевая добавка не является лекарственным средством, требуется консультация специалиста.
Введение
В последние годы коррекция дисбиоза рассматривается как одно из приоритетных направлений профилактики и лечения многих заболеваний. По определению ВОЗ, «пробиотики — это живые микроорганизмы, которые при применении в адекватных количествах вызывают улучшение здоровья организма-хозяина». Наиболее часто в качестве пробиотиков используются штаммы Lactobacillus и Bifidobacterium, кроме того, используются дрожжи Saccharomyces cerevisiae и Saccharomyces boulardii и некоторые виды Escherichia coli и Bacillus. Недавно в Европейском союзе зарегистрирован новый пищевой продукт — Clostridium butyricum [1].
Актуально исследование применения пробиотических культур в педиатрии. Показано, что олигосахариды, содержащиеся в материнском молоке, способствуют развитию бифидогенного микробиома у младенцев. Изменение состава данного микробиома может приводить к значительным функциональным расстройствам желудочно-кишечного тракта (ЖКТ) и ассоциированным с ними заболеваниям.
Функциональные нарушения ЖКТ — одна из самых распространенных проблем в детской гастроэнтерологии. По данным различных авторов, функциональные нарушения ЖКТ встречаются у 55–75% детей первых месяцев жизни. У детей раннего возраста отсутствует диагноз «функциональная абдоминальная боль». Состояние с похожими симптомами называют младенческими коликами. В первые три месяца жизни более чем у 70% детей отмечаются функциональные кишечные колики. В соответствии с Римскими критериями IV колики у младенцев представляют собой эпизоды повышенной раздражительности, беспокойства или безутешного плача, возникающие и завершающиеся без очевидных причин. Длительность младенческих кишечных колик составляет более трех часов в день и не менее трех дней в течение одной недели.
Младенческие кишечные колики характеризуются многофакторной этиологией, при этом патофизиологические механизмы, лежащие в основе кишечных колик, не установлены. Общепринято связывать их с непосредственными нарушениями функционирования ЖКТ [2]. Многофакторная этиология младенческих кишечных колик связана с различными подходами к лечению данного заболевания, включая изменение ухода за ребенком, поддержку грудного вскармливания, рациональное питание матери и медикаментозную терапию [3].
В педиатрической практике широкое применение в терапии колик нашли пеногасители, в основном препараты симетикона. Несмотря на некоторые позитивные отзывы со стороны родителей, нет достоверных доказательств в пользу пеногасителей как обезболивающего средства при кишечных коликах у младенцев [4]. Плацебо-контролируемые исследования симетикона подтверждают эти выводы [5, 6]. Сравнительные исследования пробиотиков и симетикона также показали, что симетикон неэффективен в терапии младенческих колик [7].
В терапии желудочно-кишечных нарушений у детей (в частности, при острой инфекционной диарее) довольно широко используются адсорбенты, например диосмектит. С одной стороны, метаанализ показывает, что диосмектит сокращает продолжительность диареи на один день и увеличивает шансы на полное выздоровление на третий день лечения [8]. С другой стороны, клинические рекомендации Европейского общества педиатрической гастроэнтерологии, гепатологии и нутрициологии (the European Society for Paediatric Gastroenterology Hepatology and Nutrition, ESPGHAN) подчеркивают, что комбинация диосмектита и пробиотика, содержащего Lactobacillus GG (LGG), и LGG отдельно одинаково эффективны при терапии острой инфекционной диареи у детей раннего возраста [9]. Соответственно, вопрос о сравнительной эффективности диосмектита и пробиотика остается открытым.
В последнее время состав микробиоты кишечника рассматривается как независимый фактор риска развития младенческих колик. Сравнительные исследования микрофлоры кишечника у детей с коликами и детей без колик показали значительное увеличение заселенности анаэробными грамотрицательными и грамположительными бактериями (Clostridium difficile) и снижение колонизации кишечника бактериями Lactobacillus spp. [10, 11]. Отмечено, что при тяжелых формах колик изменяется профиль жирных кислот — это также связано с лактобациллами.
Считается, что образование кишечных газов является одной из причин брюшного дискомфорта у младенцев, страдающих коликами. К главным газообразующим бактериям кишечной микрофлоры относятся Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca, Enterobacter aerogenes, Enterobacter cloacae и Enterococcus faecalis. Положительный эффект бактерий рода Lactobacillus объясняется ингибированием подобных газообразующих микроорганизмов кишечника [12].
Пробиотики при кишечной колике могут оказывать разнонаправленное действие: нормализовать микрофлору, улучшать моторику кишечника, подавлять рост патогенных микроорганизмов и усиливать барьерные функции кишечника. Пробиотики, оптимизируя микробиоценоз, одновременно корректируют другие звенья кишечного гомеостаза, связанные с микрофлорой. В клинической практике для лечения детских колик применяются бактерии рода Lactobacillus и рода Bifidobacterium. Раннее применение пребиотиков и пробиотиков у недоношенных детей может облегчать симптомы, связанные с младенческими коликами [13].
Известно, что микрофлора детей, находящихся на грудном вскармливании, значительно отличается от таковой у младенцев, получающих молочные смеси [14]. В случае раннего перевода ребенка на вскармливание искусственной смесью процесс становления микробиоценоза кишечника нарушается. Микрофлора кишечника искусственно вскармливаемых детей характеризуется повышенным содержанием бактероидов, энтеробактерий, а также более частым выделением представителей условно-патогенной флоры на фоне снижения количества бифидобактерий.
С целью воссоздания бифидогенных свойств грудного молока производители обогащают молочные смеси комплексом пре- и пробиотиков. Согласно заключению Комитета нутрициологии ESPGHAN включение в состав молочных смесей пробиотиков (по отдельности или в комбинации) безопасно и может быть ассоциировано с рядом положительных клинических эффектов, таких как снижение риска неспецифических инфекций ЖКТ, снижение частоты применения антибиотиков и меньшая частота колик и раздражения кишки [15]. У младенцев, которые получали LGG-обогащенную формулу в течение 6 мес., наблюдались более значительное увеличение роста и веса и более высокая частота дефекации, чем в группе контроля [16].
Несмотря на то, что клинические данные преимущественно свидетельствуют об эффективности пробиотических препаратов у детей с функциональными нарушениями ЖКТ, подобные исследования имеют ряд ограничений (например, размер выборки, выборочные критерии включения детей), что не дает возможности однозначной рекомендации пробиотиков при данных видах патологий. Данные обстоятельства требуют проведения дальнейших исследований.
Цель настоящего ретроспективного фармакоэпидемиологического исследования — получение дополнительных клинических данных по особенностям применения пробиотических средств у детей раннего возраста с функциональными нарушениями ЖКТ.
Материал и методы
Проведен ретроспективный анализ случайно выбранных историй болезни пациентов в возрасте до 3 лет, обратившихся за медицинской помощью и проходивших амбулаторное лечение в 7 лечебных учреждениях г. Москвы с тремя группами диагнозов: I — младенческие кишечные колики и другие функциональные нарушения ЖКТ; II — острые кишечные инфекции, ОРВИ с кишечными проявлениями, другие инфекционные заболевания; III — атопический дерматит и другие аллергические реакции.
Была сформирована база данных, включающая 502 истории болезни только тех детей, у которых были диагностированы нарушения микробиоценоза кишечника различной этиологии и присутствовали как минимум такие симптомы, как продолжительный плач и беспокойство в дневное и ночное время.
Сбор необходимых для исследования данных осуществлялся путем копирования соответствующей информации из истории болезни пациента в специально разработанную индивидуальную регистрационную карту (ИРК), в которую вносились клинико-эпидемиологические характеристики детей. Во избежание дублирования данных каждой ИРК присваивался уникальный идентификационный номер.
Критерии эффективности терапии. Эффективность терапии оценивалась по длительности симптомов заболевания (температура, диарея, рвота, боли в животе — колики, метеоризм, кожная сыпь и др.). Общая продолжительность болезни рассчитывалась как число полных дней с момента обращения к врачу до разрешения симптомов.
Дети были разделены на 3 группы в зависимости от назначенных им препаратов для ЖКТ или пробиотических продуктов:
1-я группа получала одно- и двухкомпонентные пробиотические препараты, содержащие до двух штаммов бактерий;
2-я группа получала пробиотические препараты, содержащие более двух штаммов бактерий каждый;
3-я группа не получала препараты с живыми пробиотическими бактериями, а получала другие симптоматические средства для лечения нарушений ЖКТ, например пеногасители и сорбенты.
Статистические методы. Размер выборки предварительно не рассчитывался. Данные из индивидуальных карт стационарных больных вносились в единую базу в MS Excel. Значения количественных признаков представляли в форме среднего со стандартным отклонением (M±SD) в случае нормального распределения значений или медианы и квартилей (2,5% и 97,5%). Нормальность распределения определяли по критерию Колмогорова — Смирнова. Достоверность различий средних значений определяли с использованием t-критерия для независимых выборок в случае нормального распределения значений и с применением непараметрического критерия Тьюки в иных случаях. Качественные признаки представляли в форме доли пациентов со значением данного признака от общего числа пациентов с известным значением данного признака. Доверительный интервал для доли пациентов определяли по методу Wald. Значения частоты качественных признаков в группах сравнивались с помощью критерия хи-квадрат (χ2). Достоверными считали различия при уровне значимости p≤0,05. При множественных сравнениях учитывалась поправка Бонферрони. Анализ данных проводили в пакете программ R-Studio version 1.2.1335. Результаты представлены в соответствии со стандартом STROBE. В данной работе не было условий, способных существенным образом повлиять на выводы. В связи с ретроспективным характером исследования диагнозы или патологические состояния определялись по имеющимся в медицинской документации сведениям.
Результаты исследования
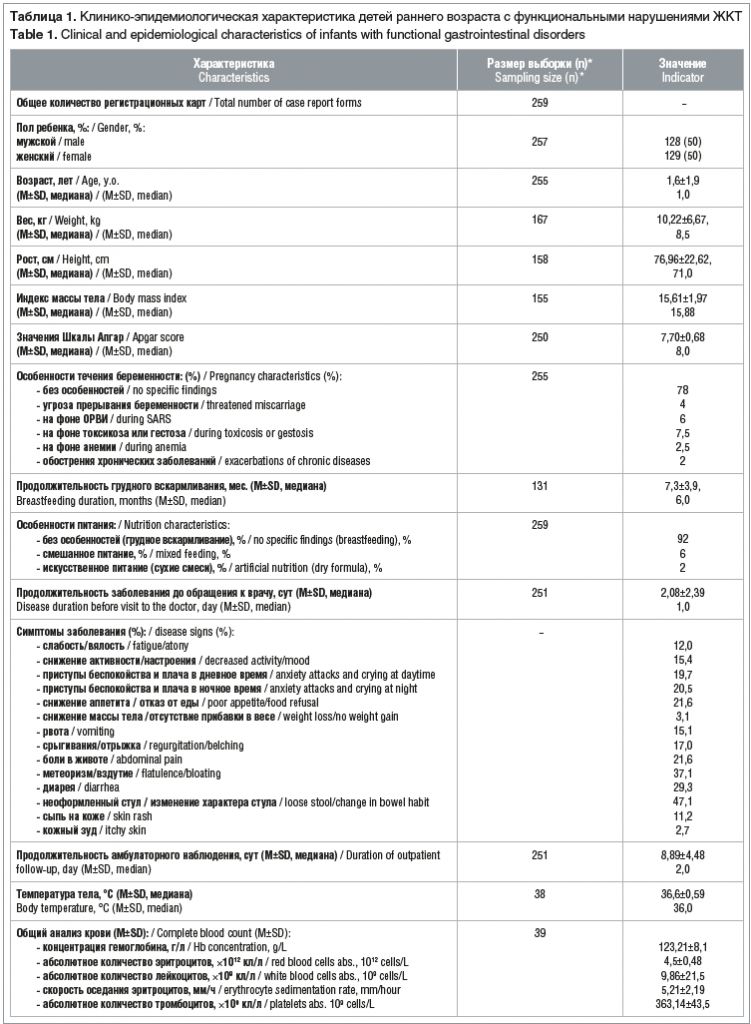
Для анализа данных по детям с функциональными нарушениями ЖКТ в исследование было включено 259 историй болезни детей раннего возраста, мальчиков и девочек поровну. Абсолютное большинство детей — 92% — получали грудное вскармливание, на смешанном питании и на сухих смесях находились 6% и 2% детей соответственно. Продолжительность симптоматики до обращения к врачу в среднем составляла 2,08±2,39 сут, среднее время, в течение которого дети находились на амбулаторном наблюдении, — 8,89±4,48 сут. Общая клинико-эпидемиологическая характеристика пациентов, включенных в исследование, приведена в таблице 1.

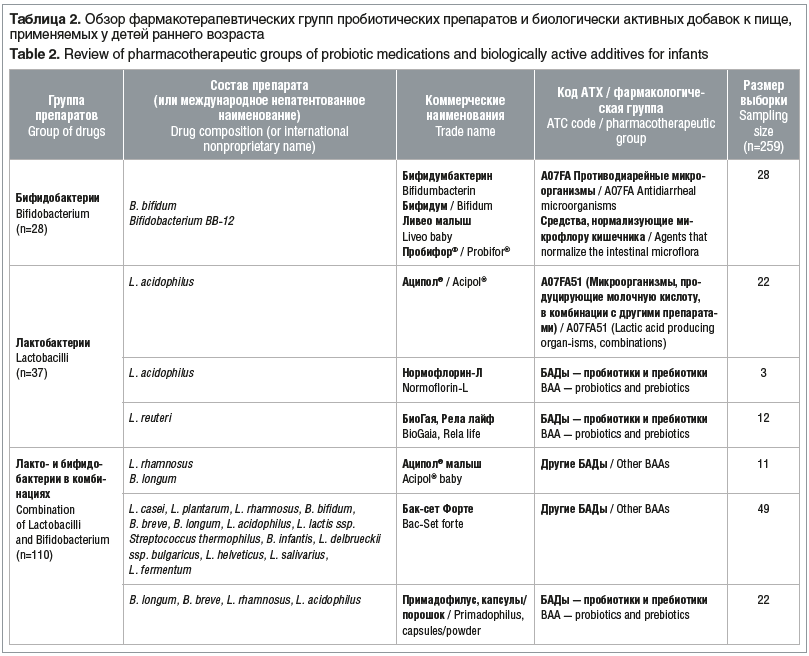
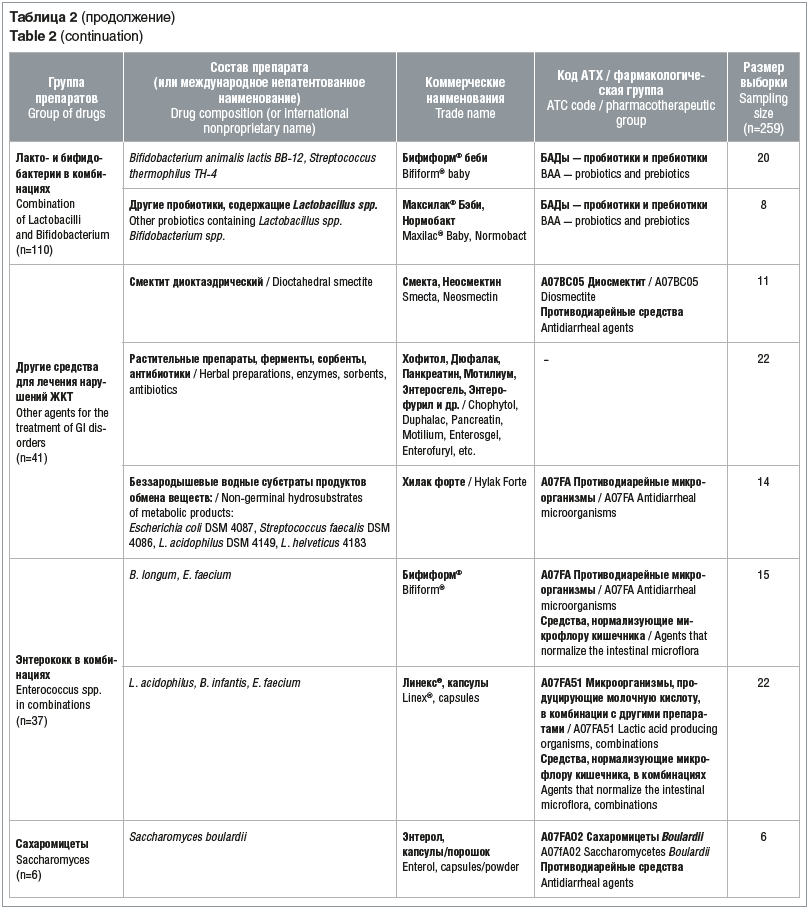
Для оценки эффективности пробиотиков в комплексной терапии функциональных нарушений ЖКТ исследуемая когорта детей была систематизирована по составу принимаемых препаратов. Из общего числа пациентов, включенных в исследование, 37 младенцев получали пробиотики из группы лактобактерий, 28 — бифидобактерии, 110 — лакто- и бифидобактерии в комбинациях, 37 — препараты энтерококков, 6 — препараты сахаромицетов и 41 младенец получал различные препараты для симптоматического лечения нарушений ЖКТ (табл. 2).
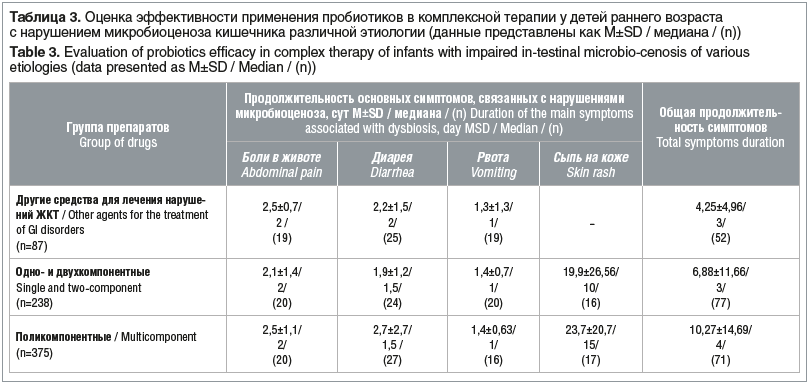
Наиболее частыми проявлениями нарушений со стороны ЖКТ были боли в животе, метеоризм, диарея и изменение консистенции стула (жидкий стул). У некоторых детей наблюдались атопические и аллергические реакции. Изменение продолжительности перечисленных симптомов рассматривалось в качестве основного показателя эффективности. Оценка эффективности различных пробиотиков представлена в таблице 3.
Оценка влияния характера питания на продолжительность симптомов, связанных с нарушением микробиоценоза кишечника, представлена на рисунке 1. Показано, что у младенцев на искусственном питании продолжительность симптомов была достоверно больше (p=0,0002).
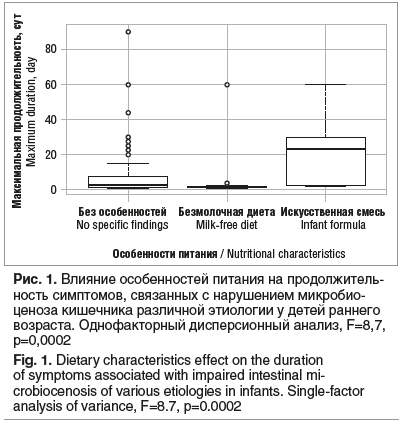
Оценка эффективности пробиотиков в комплексной терапии различных состояний, связанных с дисбактериозом, не показала значимых различий по продолжительности основных симптомов между младенцами, принимавшими различные группы пробиотиков и другие средства для терапии нарушений ЖКТ. Однако по общей максимальной продолжительности симптомов наименьшее значение показали средства для лечения нарушений ЖКТ, не содержащие в своем составе пробиотических продуктов, продолжительность симптомов в этой группе отличалась от таковой в группе поликомпонентных пробиотических препаратов (p=0,0031), но не отличалась от таковой в группе одно- и двухкомпонентных пробиотических препаратов (p=0,15). При этом наблюдалась тенденция к различию между одно- и двухкомпонентными препаратами и поликомпонентными препаратами (p=0,08).
Обсуждение
Результаты ретроспективного исследования показали разнообразие субъективных и объективных симптомов заболеваний, связанных с нарушением микробиоты кишечника и требующих применения пробиотиков у детей. При этом первостепенную роль играет тип питания ребенка. Так, в данном исследовании показано, что питание детей, включающее сухие смеси, значительно увеличивает продолжительность симптомов функциональных нарушений ЖКТ.
Известно, что тип кормления играет определяющую роль при формировании микробиоты кишечника младенцев. Так, в исследовании Baђ ckhed et al. показано, что при грудном вскармливании в микробиоте кишечника младенца преобладают бактерии рода Bifidobacterium. Также отмечается, что к возрасту 4 мес. в кишечной микробиоте младенцев на естественном вскармливании преобладают Lactobacillus johnsonii, L. gasseri, L. paracasei, L. casei и B. longum, тогда как у детей на искусственном вскармливании повышено содержание условно-патогенных бактерий: Clostridium difficile, Granulicatella adiacens, Citrobacter spp., Enterobacter cloacae, Bilophila wadsworthia [17].
Последние исследования показывают терапевтическую эффективность пробиотиков при заболеваниях, ассоциированных с изменением микрофлоры и pH кишечника, при коликах у детей, находящихся преимущественно на грудном вскармливании [7]. Исследования свидетельствуют, что повышенная заселенность кишечника бактериями рода Lactobacillus и рода Bifidobacterium является фактором защиты от развития кишечных колик и связанного с ними плача у младенцев [18]. Подобный защитный эффект может быть обусловлен тем, что бактерии Lactobacillus способны индуцировать экспрессию противовоспалительных генов [19], улучшая тем самым моторику кишечника, что в итоге ведет к снижению боли [20, 21]. Помимо этого, бактерии рода Lactobacillus и рода Bifidobacterium могут предотвращать развитие колик посредством модуляции иммунного ответа [22]. Применение пробиотиков сокращает продолжительность плача у младенцев с коликами [23].
В функциональных нарушениях ЖКТ определенную роль играют ассоциированные со специфической микробиотой процессы альтерации кишечной моторики и состояния слизистой оболочки кишечника [24]. Это обусловливает необходимость проведения более специфической (таргетной) терапии детских колик определенными видами пробиотиков, что подтверждается руководящими рекомендациями Всемирной организации гастроэнтерологов [1].
В настоящее время на фармацевтическом рынке наблюдается тенденция к формированию пула пробиотиков, содержащих широкий спектр штаммов микроорганизмов. Считается, что использование полиштаммовых пробиотиков ассоциировано с рядом преимуществ по сравнению с моноштаммовыми продуктами: 1) больший шанс на успех положительного воздействия пробиотика; 2) более широкий спектр эффективности пробиотика; 3) создание условий для синергетического эффекта (повышение адгезивных свойств различных штаммов, создание благоприятной среды, снижение антагонизма эндогенной микробиоты). С другой стороны, негативным эффектом применения комплексных пробиотиков может стать явный антагонизм между комбинированными штаммами. Штаммы в таких пробиотических комплексах могут присутствовать в разном количестве, что с точки зрения контроля качества создает проблему адекватного учета количества жизнеспособных микроорганизмов на протяжении всего срока годности продукта [25].
Иногда применение пробиотиков не позволяет добиться эффективного результата проводимой терапии [26]. Это может быть связано с тем, что гетерогенность пробиотических бактерий для организма нового хозяина может служить препятствием к их включению в состав резидентной микрофлоры. Кроме того, отмечается рост числа побочных эффектов, особенно в сенсибилизированном организме, поскольку гетерогенная микробная масса препарата, а иногда и дополнительно включенные в его состав компоненты могут давать значительную антигенную нагрузку на организм [26].
В настоящее время изучается вопрос о возможности лабораторного прогнозирования результатов лечения пробиотиками. Известно, что пробиотические штаммы могут по-разному взаимодействовать с собственной микрофлорой кишечника. Известны механизмы, посредством которых пробиотические бактерии могут воздействовать на микробиоту человека. Эти механизмы включают: конкуренцию за питательные вещества в качестве субстратов для роста; биоконверсию; производство субстратов (например, витаминов) для роста других бактерий; прямой антагонизм (с помощью бактериоцинов); конкуренцию за связывание с кишечной стенкой; улучшение барьерной функции; уменьшение воспаления; стимуляцию врожденного иммунного ответа (механизмы до конца не известны) [27]. Индивидуальный подбор монокомпонентных пробиотиков путем тестирования упрощает прогнозирование результатов лечения. В случае же с поликомпонентным пробиотиком результат лечения трудно прогнозировать, так как суммировать взаимодействие штаммов препарата с аутохтонной флорой практически невозможно. Кроме того, в одном препарате положительное действие одних штаммов может сочетаться с угнетающим действием других штаммов на собственную микрофлору пациента.
Помимо этого, пробиотики могут вырабатывать биогенные амины (гистамин, тирамин, 2-фенилэтиламин, путресцин, кадаверин), высокие количества которых вызывают головную боль, учащенное сердцебиение, рвоту, диарею, гипертензивные кризы и другие негативные эффекты [28]. При этом чем больше в пробиотическом препарате штаммов, продуцирующих биогенные амины, тем больше вероятность возникновения побочных эффектов, которые при этом не всегда можно связать с приемом пробиотиков, но которые вызывают дискомфорт.
В недавнем систематическом обзоре и метаанализе сравнительной эффективности полиштаммовых и моноштаммовых пробиотиков было показано, что в большинстве случаев отдельные штаммы эквивалентны комбинациям [29]. Выбор подходящего пробиотика должен основываться не на количестве штаммов в продукте, а на результатах доказательных исследований препаратов.
Результаты нашего исследования согласуются с выводами, что одно- и двухкомпонентные пробиотики не уступают по эффективности и могут быть более предпочтительными по сравнению с комбинированными препаратами за счет тех недостатков у последних, которые перечислены выше.
Заключение
Комплексная терапия пробиотиками обоснована при широком спектре нозологий. Постоянно расширяется применение данных препаратов, открываются новые их возможности в терапии различных заболеваний. Однако, как было показано в данном исследовании, необходим рациональный подход к назначению таргетной терапии пробиотиками. Поликомпонентные пробиотические препараты не всегда обладают преимуществами по сравнению с монокомпонентными. Более того, они имеют ряд недостатков, таких как избыточная антигенная нагрузка на слизистую ЖКТ, конкурентное взаимодействие штаммов. В связи с этим при назначении пробиотической терапии функциональных нарушений ЖКТ у детей раннего возраста предпочтение следует отдавать монокомпонентным препаратам. В настоящее время наиболее эффективными при терапии функциональных нарушений ЖКТ у младенцев и других нарушений, связанных с дисбактериозом, считаются пробиотики, содержащие бактерии L. rhamnosus, L. reuteri, L. casei, L. bulgaricus, L. acidophilus, а также B. longum и B. animalis [30].
Благодарность
Авторы и редакция благодарят компанию АО «ОТИСИФАРМ» за предоставление полных текстов иностранных статей, требовавшихся для подготовки обзорной части данной публикации.
Acknowledgement
The authors and Editorial Board are grateful to «OTCPharm» JSC for providing full-text foreign articles required to write the review.
Сведения об авторах:
Блохин Борис Моисеевич — д.м.н., профессор, заведующий кафедрой поликлинической и неотложной педиатрии педиатрического факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0003-4762-5975.
Прохорова Анастасия Дмитриевна — ассистент кафедры поликлинической и неотложной педиатрии педиатрического факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-9028-7791.
Лобушкова Ирина Павловна — к.м.н., доцент кафедры поликлинической и неотложной педиатрии педиатрического факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0003-2690-676X.
Суюндукова Алия Сагитовна — к.м.н., доцент кафедры поликлинической и неотложной педиатрии педиатрического факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-4369-4300.
Гордиенко Галина Иосифовна — к.м.н., доцент кафедры поликлинической и неотложной педиатрии педиатрического факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-2966-6696.
Стешин Вадим Юрьевич — к.м.н., доцент кафедры поликлинической и неотложной педиатрии педиатрического факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0002-2279-2577.
Кагирова Зарема Руслановна — ассистент кафедры поликлинической и неотложной педиатрии педиатрического факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0001-9002-7909.
Мирзоев Тахир Ханафиевич — к.м.н., доцент кафедры поликлинической и неотложной педиатрии педиатрического факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0003-3126-2380.
Мельникова Марина Анатольевна — к.м.н., ассистент кафедры поликлинической и неотложной педиатрии педиатрического факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD ORCID iD 0000-0002-5342-622X.
Антипова Надежда Владимировна — ассистент кафедры поликлинической и неотложной педиатрии педиатрического факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 117997, Россия, г. Москва, ул. Островитянова, д. 1; ORCID iD 0000-0001-6950-2584.
Контактная информация: Блохин Борис Моисеевич, e-mail: blokhinb@gmail.com. Конфликт интересов отсутствует. Прозрачность финансовой деятельности: авторы не имеют финансовой заинтересованности в представленных материалах или методах. Статья поступила 14.09.2020, поступила после рецензирования 05.10.2020, принята в печать 19.10.2020.
About the authors:
Boris M. Blokhin — Dr. of Sci. (Med.), Professor, Head of the Department of Outpatient and Emergency Pediatrics, Faculty of Pediatrics, Pirogov Russian National Research Medical University: 1, Ostrovityanova str., Moscow, 117997, Russian Federation; ORCID iD 0000-0003-4762-5975.
Anastasia D. Prokhorova — Assistant Professor of the Department of Outpatient and Emergency Pediatrics, Faculty of Pediatrics, Pirogov Russian National Research Medical University: 1, Ostrovityanova str., Moscow, 117997, Russian Federation; ORCID iD 0000-0002-9028-7791.
Irina P. Lobushkova — Cand. of Sci. (Med.), Associate Professor of the Department of Outpatient and Emergency Pediatrics, Faculty of Pediatrics, Pirogov Russian National Research Medical University: 1, Ostrovityanova str., Moscow, 117997, Russian Federation; ORCID iD 0000-0003-2690-676X.
Aliya S. Suyundukova — Cand. of Sci. (Med.), Associate Professor of the Department of Outpatient and Emergency Pediatrics, Faculty of Pediatrics, Pirogov Russian National Research Medical University: 1, Ostrovityanova str., Moscow, 117997, Russian Federation; ORCID iD 0000-0002-4369-4300.
Galina I. Gordiyenko — Cand. of Sci. (Med.), Associate Professor of the Department of Outpatient and Emergency Pediatrics, Faculty of Pediatrics, Pirogov Russian National Research Medical University: 1, Ostrovityanova str., Moscow, 117997, Russian Federation; ORCID iD 0000-0002-2966-6696.
Vadim Yu. Steshin — Cand. of Sci. (Med.), Associate Professor of the Department of Outpatient and Emergency Pediatrics, Faculty of Pediatrics, Pirogov Russian National Research Medical University: 1, Ostrovityanova str., Moscow, 117997, Russian Federation; ORCID iD 0000-0002-2279-2577.
Zarema R. Kagirova — Assistant Professor of the Department of Outpatient and Emergency Pediatrics, Faculty of Pediatrics, Pirogov Russian National Research Medical University: 1, Ostrovityanova str., Moscow, 117997, Russian Federation; ORCID iD 0000-0001-9002-7909.
Takhir Kh. Mirzoev — Cand. of Sci. (Med.), Associate Professor of the Department of Outpatient and Emergency Pediatrics, Faculty of Pediatrics, Pirogov Russian National Research Medical University: 1, Ostrovityanova str., Moscow, 117997, Russian Federation; ORCID iD 0000-0003-3126-2380.
Marina A. Melnikova — Cand. of Sci. (Med.), Assistant Professor of the Department of Outpatient and Emergency Pediatrics, Faculty of Pediatrics, Pirogov Russian National Research Medical University: 1, Ostrovityanova str., Moscow, 117997, Russian Federation; ORCID iD 0000-0002-5342-622X.
Nadezhda V. Antipova — Assistant Professor of the Department of Outpatient and Emergency Pediatrics, Faculty of Pediatrics, Pirogov Russian National Research Medical University: 1, Ostrovityanova str., Moscow, 117997, Russian Federation; ORCID iD 0000-0001-6950-2584.
Contact information: Boris M. Blokhin, e-mail: blokhinb@gmail.com. There is no conflict of interest. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. Received 14.09.2020, revised 05.10.2020, accepted 19.10.2020.
Рейтинг 5.00 из 5 на основе опроса 1 пользователя
(1 отзыв клиента)
77 руб. – 204 руб.
- Описание
- Детали
- Отзывы (1)
Описание
Скорая помощь при болях в животе – тайская эмульсия «Летающий белый кролик»
Эмульсия от отравлений и болей в животе под названием «Летающий белый кролик» — эффективное и быстрое средство от боли и спазмов в животе, от диареи, тошноты и рвоты. Эмульсия «Летающий белый кролик» известна в Таиланде уже более 70 лет, это настоящая скорая помощь для путешественников или для любителей отдыха на природе при отравлениях и неприятных ощущениях в животе.
Тайское средство «Летающий кролик» практически за 20 минут снимает неприятные и болезненные ощущения в животе, спазмы, колики, тошноту и сразу же остановит диарею.
Эмульсия имеет приятный мятный вкус.
Состав тайской эмульсии «Белый кролик» на каждые 100 мл:
- Салол 2 грамма – антисептическое, жаропонижающее и противовоспалительное действия.
- Анисовое масло 0,132 мл – снимает спазмы в кишечнике, устраняет боль в животе, способствует пищеварению, ускоряет перистальтику и устраняет газообразование
- Ментол 0,176 грамм – общий антисептик, улучшает работу желудка, снимает тошноту, обладает противоспазматическим и глистогонным действием.
Тайское средство Летающий белый кролик применяют:
- При пищевых и алкогольных отравлениях
- При болях в желудке и кишечнике
- При диарее, тошноте, рвоте и изжоге
- При энтероколите и колите
- Эмульсию можно принимать детям
Способ применения эмульсии «летающий белый кролик»:
- Взболтать, взрослым — 1 столовая ложка, детям 1-2 чайные ложки, не запивать
- Через 20 минут при необходимости можно повторить прием тайской эмульсии от отравления
- Хранить при комнатной температуре (не хранить в холодильнике)
Противопоказания к применению: Аллергия к любому из компонентов эмульсии
Объем эмульсии против отравления и боли в животе — на Ваш выбор:
- Эмульсия Летающий кролик 50 мл
- Эмульсия Летающий кролик 200 мл
Детали
| Вес | Н/Д |
|---|---|
| Объем |
200 мл, 50 мл |
Только зарегистрированные клиенты, купившие этот товар, могут публиковать отзывы.
Здравствуйте, дорогие читатели!
Перед поездкой в новую страну, наверняка, многие изучают информацию о том, что оттуда стоит привезти. Так вот из Тае «сувенирами» лучше закупаться в аптеках, а не в сувенирных лавках, особенно это касается полуострова Пхукета. Поэтому в списке необходимых покупок у меня сразу был Летающий кролик, расхваливаемый множеством интернет-ресурсов, а так же блогерами.
Эмульсия Thaipharmed Летающий белый кролик Flying Rabbit
Где купить Аптеки Тайланда
Цена ок.150 рублей
Обьем 200 мл
Производитель Тайланд
Состав:
— Салол 2 гр – антисептическое, жаропонижающее и противовоспалительное действия;
— Анисовое масло 0,132 мл – снимает спазмы в кишечнике, устраняет боль в животе, способствует пищеварению, ускоряет перистальтику и устраняет газообразование;
— Ментол 0,176 гр – общий антисептик, улучшает работу желудка, снимает тошноту, обладает противоспазматическим и глистогонным действием.
? ВНЕШНИЙ ВИД
Довольно узнаваемая уже бутылочка, бело-зеленого цвета, выполненная из прозрачного пластика. Половина надписей на английском, половина на тайском.
Средство очень популярно на родине, но, видимо, туристы расхватывают его с не меньшим рвением, поэтому и появился перевод. Понятных нам надписей довольно мало, но вполне хватает, что бы примерно понять, что там внутри, как это принимать и для чего.
Есть даже сроки годности, аж 4 года. Полного состава я не нашли, лишь активные компоненты, поэтому не представляю, что в эмульсии содержится для ее сохранения.
Так же обратите внимание, на надпись:
must not be refrigerated
Она предупреждает нас, что охлаждать препарат не нужно, т.е. хранение в холодильнике не нужно, я ставлю его просто в аптечку.
Есть небольшая табличка, где указано сколько мл или грамм содержится активного компонента в 100 мл эмульсии. Тут мы видим анисовое масло и ментол — третий компонент мне не известен.
Бутылочка очень простая, полностью прозрачная, у меня обьем 200 мл, видела, было и 50 мл в продаже. Крышечка металлическая, закручивающаяся, опять же с изображением белого кролика. Никаких примудростей, но главное все плотно закрывается и ничегошеньки не вытекает.

Эмульсия белого цвета, однородной консистенции, без каких-либо вкраплений, осадка не появляется при хранении. Аромат насыщенный, ментоловый.
? ОПИСАНИЕ
Так как препарат можно найти даже у нас в интернет-магазинах, то и описание к нему уже полагается в них на русском языке.
Эмульсия «Летающий белый кролик» – это эффективное и быстрое средство от отравлений, от боли и спазмов в животе, от диареи, тошноты и рвоты. Эмульсия «Летающий белый кролик» известна в Таиланде уже более 70 лет, это настоящая скорая помощь при отравлениях и неприятных ощущениях в животе.
Для чего можно использовать эмульсию — указано на бутылочке на английском языке, собственно, это показания привычные нам — что то вроде нашей смекты или энтеросгеля.
Аромат мятный, собственно как и вкус, чем то очень напоминает зубную пасту, все же мята «насыщенная».
Тайское средство «Летающий белый кролик» применяют:
— при пищевых и алкогольных отравлениях;
— при болях в желудке и кишечнике;
— при диарее, тошноте, рвоте и изжоге;
— при энтероколите и колите.
Противопоказаний не указано, разве что если есть аллергия на один из компонентов эмульсии.
На бутылочке так же указан официальный сайт производителя, вот прямая ссылка на товар:
Летающий кролик — информации тут не намного больше, но мы уже видим, что данная компания выпускает и другие продукты, в основном витамины.
? ПРИМЕНЕНИЕ
По инструкции все просто — взбалтываем бутылочку, принимаю по 1 ложке, у меня что-то между столовой и чайной.
Через пол часа повторяю.
Мне двух ложек хватает, что бы самочувствие пришло в норму.
А теперь важная информация:
❗❗❗ С КАКОГО ВОЗРАСТА МОЖНО ПРИНИМАТЬ ЛЕТАЮЩЕГО КРОЛИКА ❗❗❗
Увы, на флаконе и на сайте такой информации нет, а зря, ведь не узнав это случайно в тайской аптеке, могла бы и дать эмульсию своей трехлетней дочери.
Итак, Летающего кролика можно пить с 6 лет. Видимо, было в аптеках много вопросов на этот счет, а местные фармацевты не говорят по русски, поэтому прямо под ценником в аптеке и было описано это ограничение для наших соотечественников (на других языках не было).

У нас не бывает отравлений и прочего описанного по описанию, единственное, для чего я применяю Летающего кролика — возможная интоксикация после употребления алкоголя. Увы, частенько получается так, что даже после двух бокалов шпанского или вина, у меня появляются неприятные ощущения в животе на утро. Предполагаю, связано это с тем, с какой едой все это употребляется.
Вообщем, когда выдалось то самое, «неудачное» утро — я принимаю 2 ложки эмульсии раз в пол часа. Запиваю 1/2 стакана воды.
? РЕЗУЛЬТАТ
Первое, что хочу отметить — эффективнгосьт тайской эмульсии превзошли нашу Смекту и Энтеросгеля.
Облегчение приходит гораздо быстрее, действительно за 15-30 минут, и применять ее горазо приятнее, пусть и кажется, что пьешь зубную пасту
Всего 2 ложки снимают
▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬▬
█ ▌ ВЫВОДЫ
Единственное, о чем пожалела — купила всего бутылочку, но очень обрадовалась, что Летающего кролика можно найти и у нас в России, весь сейчас такйские магазиники довольно распространены, и вдвойне приятно, что цена не выше местной. Я, например, нашла 200 мл за 200 рублей. Расход очень экономный, поэтому хватит мне ее на пол года точно.
Очень простой состав, удобство применения, доступность на нашем рынке — все это делает Летающего кролика №1 простив отравлений.
☑ эффективное средство от тошноты
☑ отлично помогает при отравлениях
☑ удобный прием — всего по 1 ложке
☑ быстро справляется со своей задачей
☑ можно принимать детям с 6 лет
☑ экономичный расход
☑ низкая цена
☑ можно купить не только в Тае, но и в наших специализированных тайских интернет-магазинах
☒ специфический вкус и насыщенный ментоловый аромат
РЕКОМЕНДУЮ!
ღ๑♥●•· До новых встреч! ●♥•°•ღ
Для эффективной борьбы с тошнотой, рвотой, диареей и дискомфортными ощущениями в области эпигастрии в традиционной медицине часто используется эмульсия Белый кролик. Это тайское лекарство, которое хорошо известно путешественникам, так как в походных условиях это средство является незаменимым.
Всего за 15-20 мин. эмульсия помогает устранить болезненные ощущения в животе, а также побороть спазмы и колики в кишечнике. В состав препарата входят компоненты, которые являются безопасными как для взрослых, так и для детей.
Перед покупкой лекарственного средства необходимо проконсультироваться с гастроэнтерологом и изучить инструкцию по применению, чтобы снизить вероятность возникновения побочных реакций.
Форма выпуска и состав эмульсии
Белый кролик – тайское лекарство, которое эффективно при алкогольных и пищевых отравлениях. Препарат выпускается в форме эмульсии, которая реализуется в банках из прочного пластика по 50 или 200 мл.
Высокая эффективность лекарственного средства обусловлена тем, что в его составе присутствуют сразу 3 активных компонента, которые положительно влияют на работу органов пищеварительной системы и существенно улучшают состояние больного.
| Название компонента | Свойства |
| Фенилсалицилат (салол) | Это фениловый эфир салициловой кислоты, который оказывает на организм пациента противовоспалительное и антисептическое действие. При пероральном применении вещество не меняет своих характеристик под воздействием желудочного сока. Фенилсалицилат помогает побороть патогенную микрофлору, а также оказывает жаропонижающее и противовоспалительное действие. Выводится вещество естественным путем (вместе с уриной) в неизмененном виде. В фармакологии салол включают в состав комбинированных лекарственных средств, которые пользуются спросом в гастроэнтерологии. |
| Анисовое масло | Это мощное антиспазматическое вещество, которое улучшает пищеварение, а также оказывает ветрогонное действие. |
| Ментол | Этот компонент улучшает работу органов ЖКТ, а также обладает глистогонным и противоспазматическим действием. Ментол показан при атонии кишечника, гастрите, энтероколите, метеоризме, спазмах кишечника и желудка, холецистите, рвоте, тошноте, а также при наличии конкрементов в почках и желчном пузыре. |
При правильном применении тайское лекарство помогает побороть болезненную симптоматику без вреда для здоровья. Медицинская статистика подтверждает, что препарат хорошо переносится организмом пациентов разных возрастов.
Фармакологические свойства
Белый кролик – тайское лекарство, которое эффективно в борьбе с энтероколитом и колитом у детей и взрослых. В состав препарата входят компоненты, которые обволакивают стенки желудка и кишечника, благодаря чему существенно возрастает жизнеспособность эпителиальных клеток слизистой оболочки желудочно-кишечного тракта.
Под действием соляной кислоты формируется максимально прочный полимерный слой, соединенный с белковыми экссудатами, который играет роль защитного барьера.
Эмульсия Белый кролик помогает связать пепсин и желчные кислоты, которые попадают в желудок при развитии рефлюкс-эзофагита. Препарат позволяет добиться цитопротективного эффекта, благодаря чему происходит стимуляция эндогенных простагландинов. Дополнительно тайское лекарство улучшает кровоснабжение слизистой оболочки органов ЖКТ.
Только при отсутствии патологий пищеварительной системы в желудке синтезируется муцин. Это специальная слизь, которая помогает защитить слизистую оболочку органов ЖКТ от агрессивной кислой среды выделяемого желудочного сока. Если муцин не вырабатывается в необходимом количестве, то это чревато образованием язв и эрозий на слизистой оболочке.
Показания к применению
Белый кролик всего за 10-20 мин. устраняет острую боль в желудке и кишечнике. Тайское лекарство также помогает организму быстрее восстановиться при пищевых отравлениях.
В инструкции к препарату указаны следующие показания к применению:
- Метеоризм.
- Спазмы желудка и кишечника.
- Гастрит.
- Атония кишечника.
- Тошнота, рвота.
- Наличие конкрементов в почках или желчном пузыре.
- Холецистит.
- Диарея.
- Рефлюкс-эзофагит.
- Пищевые и алкогольные отравления.
- Бактериальный энтероколит.
- Язва желудка и двенадцатиперстной кишки.
Лекарственное средство Белый кролик часто включают в состав комплексной медикаментозной терапии, когда плохое самочувствие пациента спровоцировал рецидив хронического заболевания желудочно-кишечного тракта.
Противопоказания
Белый кролик – эффективное лекарство широкого спектра действия, применять которое можно только после предварительной консультации с квалифицированным гастроэнтерологом.
Препарат запрещено использовать при повышенной чувствительности организма к входящим в состав эмульсии компонентам. Лекарственное средство Белый кролик не назначают тем пациентам, которые обладают повышенной чувствительностью к фенолам и салицилатам.
Тайский препарат также нельзя принимать при наличии следующих заболеваний и состояний:
- Тяжелая форма почечной или печеночной недостаточности.
- Беременность.
- Период лактации.
- Артериальная гипотензия.
- Детский возраст.
Для эффективной борьбы с заболеваниями желудочно-кишечного тракта и устранения болезненной симптоматики перед покупкой медикаментозных препаратов нужно пройти ультразвуковое исследование органов брюшной полости. Только гастроэнтеролог может назначить безопасную и результативную схему лечения, которая не спровоцирует прогрессирование диагностированной патологии.
С какого возраста можно применять тайское лекарство?
Тайское лекарство Белый кролик можно использовать для устранения дискомфортных ощущений в желудке и кишечнике у детей старше 6 лет. Целесообразность применения препарата в более раннем возрасте должны оценивать гастроэнтеролог и педиатр, руководствуясь общей клинической картиной. Лечение заболеваний органов ЖКТ у детей всех возрастных групп должно проходить под контролем лечащего врача.
Инструкция по применению, дозировка
Самолечение пищевых отравлений и патологий органов желудочно-кишечного тракта чревато стремительным ухудшением самочувствия больного. Неправильно подобранная схема лечения может спровоцировать развитие сопутствующих заболеваний и усиление имеющейся болезненной симптоматики.
Длительность терапевтического курса и кратность применения препарата Белый кролик должен определять гастроэнтеролог. Крайне опасным является самолечение при сильном пищевом либо алкогольном отравлении, так как больной должен быть госпитализирован.
Взрослым
Перед употреблением лекарственное средство Белый кролик обязательно нужно взболтать. Взрослым пациентам рекомендуется принимать по 1 ст. л. эмульсии 1 раз в сутки. Длительность терапевтического курса определяется индивидуально, так как все зависит от состояния пациента.
Если плохое самочувствие вызвано алкогольным или пищевым отравлением, тогда нужно принять 1 ст. л. тайской эмульсии, а через 30 мин. снова употребить такую же дозу препарата. Лекарственное средство не нужно запивать.
Детям
Для лечения заболеваний органов ЖКТ или устранения последствий пищевого отравления у детей старше 6 лет рекомендуется принимать по 1-2 ч. л. эмульсии 1 раз в сутки. Длительность терапевтического курса должен определить гастроэнтеролог либо педиатр. После применения препарата в течение 1 ч. запрещено есть и пить.
Побочные действия
В 98% случае тайское лекарство Белый кролик хорошо переносится организмом взрослых и детей. Только в единичных случаях состояние пациентов ухудшается, что связано с несоблюдением рекомендуемой схемы лечения.
К возможным побочным реакциям относятся следующие симптомы:
- Бессонница.
- Головная боль.
- Головокружение.
- Учащенное сердцебиение.
- Снижение показателей артериального давления (гипертензия).
- Тошнота.
- Запор.
- Аллергические реакции (например, крапивница, ангионевротический отек, высыпания на кожном покрове).
При возникновении побочных реакций нужно прекратить принимать эмульсию и обратиться за консультацией к лечащему врачу, который поможет подобрать более безопасный и эффективный аналог.
Передозировка
В медицинской практике пока не были зафиксированы случаи передозировки лекарственным средством Белый кролик.
Но по причине систематического превышения допустимой дозировки препарата у больного могут возникнуть следующие симптомы:
- Мигрень.
- Тошнота, рвота.
- Раздражительность.
- Общее недомогание, озноб.
- Повышение температуры тела.
- Спутанность сознания.
- Дискомфортные ощущения в области эпигастрии.
- Запор.
- Отек Квинке.

Особые указания
Белый кролик – тайское лекарство, которое отлично справляется с холециститом и метеоризмом с минимальным риском возникновения побочных реакций.
В единичных случаях компоненты препарата могут вызывать головокружение и головные боли, из-за чего в течение 4 ч. после применения эмульсии не рекомендуется управлять автомобилем и сложными механизмами, которые требуют повышенной концентрации внимания.
В лабораторных условиях не были проведены необходимые исследования по поводу того, как фенилсалицилат, ментол и анисовое масло влияют на организм еще не рожденного ребенка. По этой причине в период беременности не рекомендуется принимать средство Белый кролик для нормализации работы органов ЖКТ.
Для устранения болезненной симптоматики в пищеварительном тракте женщина должна пройти комплексное медицинское обследование, так как только в этом случае врач сможет оценить соотношение потенциальной пользы медикаментозного лечения для будущей матери и возможного риска для плода.
Лекарственное взаимодействие
Эмульсию Белый кролик можно включать в состав комплексной медикаментозной терапии, действие которой направлено на нормализацию работы желудка и кишечника. При наличии у больного хронических патологий печени, почек или сердца безопасность применения сразу нескольких лекарственных средств должен оценивать лечащий врач, так как каждый случай является индивидуальным.
Аналоги
Принимать лекарственное средство Белый кролик можно только при отсутствии противопоказаний. В противном случае препарат нужно заменить. Среди доступных аналогов тайской эмульсии можно выделить те лекарственные средства, которые помогают устранить болезненную симптоматику и улучшают работу органов ЖКТ.
| Название препарата | Описание |
| Анацид | Препарат комплексно воздействует на организм больного при медикаментозном лечении заболеваний желудочно-кишечного тракта. Анацид имеет следующие показания к применению: рвота, изжога, язвенная болезнь желудка и двенадцатиперстной кишки, нарушение секреции желудочного сока. Среди противопоказаний можно выделить только повышенную чувствительность организма к компонентам препарата. Принимать Анацид рекомендуется по 1-2 таблетки 2 раза в сутки за 30 мин. до еды. Длительность лечения определяется индивидуально. |
| Маалокс | Этот препарат предназначен для лечения следующих патологий: хронический и острый гастродуоденит, язва желудка или двенадцатиперстной кишки, рефлюкс-эзофагит, диафрагмальная грыжа, болезненные ощущения в области эпигастрии, диспептические явления. Противопоказания: гипофосфатемия, почечная недостаточность, индивидуальная непереносимость мальтитола, детский возраст (до 15 лет). Таблетки нужно рассасывать либо разжевывать. Взрослым и детям старше 15 лет Маалокс прописывают в дозировке 1-2 таблетки 3-4 раза в день. Препарат рекомендуется принимать за 2 ч. до еды. Терапевтический курс назначается гастроэнтерологом индивидуально для каждого пациента. |
| Гелусил | Лекарственное средство обладает высокой эффективностью в борьбе с острым дуоденитом, грыжей пищеводного отверстия диафрагмы, язвенной болезнью желудка и двенадцатиперстной кишки. Гелусил можно использовать для симптоматического лечения тяжести и боли в области эпигастрии, а также при изжоге. Препарат противопоказан при непереносимости сималдрата, хронической почечной недостаточности, болезни Альцгеймера, а также в период беременности. Принимать суспензию Гелусил нужно 2-3 раза в сутки по 10 мл через 60 мин. после еды. Если терапевтический эффект недостаточен, тогда гастроэнтеролог может увеличить дозировку препарата. Длительность лечения зависит от состояния больного. |
Перед покупкой любого медикаментозного средства следует проконсультироваться с лечащим врачом, так как самолечение патологий ЖКТ чревато стремительным ухудшением самочувствия больного и снижением качества его жизни.
Сроки, условия продажи и хранения
Тайскую эмульсию Белый кролик можно купить без рецепта врача. Хранить лекарственное средство нужно в сухом, недоступном для прямых солнечных лучей месте.
Температура воздуха в помещении должна быть в пределах от +17 до +27 C. Запрещено ставить банку с эмульсией в холодильник. Срок годности препарата составляет 4 года.
Цена эмульсии Белый кролик
Купить тайское лекарство Белый кролик можно в интернет-магазинах. Но для покупки эмульсии рекомендуется выбирать только проверенные точки сбыта, чтобы случайно не купить фальсифицированный товар. Средняя стоимость препарата варьируется в пределах от 190 до 300 руб.
Видео о препарате Белый кролик
Белый кролик быстро лечит живот:
Эмульсия «Белый Летающий Кролик» (тайское лекарство снимает спазмы, колики, тошноту, остановит диарею), 50 или 200 мл
Скорая помощь при болях в животе – эмульсия «Летающий белый кролик» — Flying Rabbit (тайское лекарство снимает спазмы, колики, тошноту, остановит диарею).
Объем — 50 мл (вес брутто — 58 гр)
или 200 мл (вес брутто — 217 гр)
Скорая помощь при болях в животе – эмульсия «Летающий белый кролик» — Flying Rabbit (тайское лекарство снимает спазмы, колики, тошноту, остановит диарею).
Объем — 50 мл (вес брутто — 58 гр)
или 200 мл (вес брутто — 217 гр)
Эмульсия от отравлений и болей в животе под названием «Летающий белый кролик» — эффективное и быстрое средство от боли и спазмов в животе, от диареи, тошноты и рвоты. Эмульсия «Летающий белый кролик» известна в Таиланде уже более 70 лет, это настоящая скорая помощь для путешественников или для любителей отдыха на природе при отравлениях и неприятных ощущениях в животе.
Тайское средство «Летающий кролик» практически за 20 минут снимает неприятные и болезненные ощущения в животе, спазмы, колики, тошноту и сразу же остановит диарею.
Эмульсия имеет приятный мятный вкус.
Купить эмульсию Белый Летающий Кролик (тайское лекарство снимает спазмы, колики, тошноту, остановит диарею), инструкция по применению OrganicThai прямо из Тайланда.
Состав тайской эмульсии «Белый кролик» на каждые 100 мл:
- Салол 2 грамма – антисептическое, жаропонижающее и противовоспалительное действия.
- Анисовое масло 0,132 мл – снимает спазмы в кишечнике, устраняет боль в животе, способствует пищеварению, ускоряет перистальтику и устраняет газообразование
- Ментол 0,176 грамм – общий антисептик, улучшает работу желудка, снимает тошноту, обладает противоспазматическим и глистогонным действием.
Тайское средство Летающий белый кролик применяют:
- При пищевых и алкогольных отравлениях
- При болях в желудке и кишечнике
- При диарее, тошноте, рвоте и изжоге
- При энтероколите и колите
- Эмульсию можно принимать детям.
Эмульсия Белый Летающий Кролик (тайское лекарство) — инструкция по применению:
- Взболтать, взрослым — 1 столовая ложка, детям 1-2 чайные ложки, не запивать;
- Через 20 минут при необходимости можно повторить прием тайской эмульсии от отравления.
Противопоказания к применению: Аллергия к любому из компонентов эмульсии.
Хранить при комнатной температуре.
НЕЛЬЗЯ ХРАНИТЬ В ХОЛОДИЛЬНИКЕ!
Нет комментариев
Добавить комментарий
Тайская Эмульсия Flying Rabbit Abdominal Pain Flatulence Diarrhea Инструкция По Применению
Эмульсия Летающий белый кролик – это эффективное и быстрое средство от отравлений, от боли и спазмов в животе, от диареи, тошноты и рвоты. Эмульсия Flying Rabbit известна в Таиланде уже более 70 лет, это настоящая скорая помощь при отравлениях и неприятных ощущениях в животе.
Тайское средство Летающий кролик практически за 20 минут снимает неприятные и болезненные ощущения в животе, спазмы, колики, тошноту и сразу же останавливает диарею.
Эмульсия имеет приятный мятный вкус.
Активные вещества в составе эмульсии, в 100 мл.
- Салол 2 гр. – антисептическое, жаропонижающее и противовоспалительное действие;
- Анисовое масло 0,132 мл. – снимает спазмы в кишечнике, устраняет боль в животе, способствует пищеварению, ускоряет перистальтику и устраняет газообразование;
- Ментол 0,176 гр. – общий антисептик, улучшает работу желудка, снимает тошноту, обладает противоспазматическим и глистогонным действием.
Показания к применению
- пищевые и алкогольных отравленя;
- боли в желудке и кишечнике;
- при диарее, тошноте, рвоте и изжоге;
- при энтероколите и колите.
Способ применения
Перед применением бутылочку с эмульсией взболтать.
Взрослым
- 1 столовая ложка
Детям
- 1-2 чайные ложки
Средство Flying Rabbit abdominal pain не требует запивания.
Через 20 минут при необходимости можно повторить прием препарата.
Способ хранения
Хранить при комнатной температуре, в темном месте, не доступным детям.
Противопоказания
Индивидуальная непереносимость.
Объем: 50/200 мл. на Ваш выбор
Препарат сертифицирован и продается в аптеках Таиланда без рецепта. Перед применением требуется консультация специалиста.
Синдром раздраженного кишечника (СРК) является хроническим рецидивирующим и функциональным расстройством желудочно-кишечного тракта (ЖКТ). В прошлом синдром раздраженного кишечника рассматривался как диагноз исключения. В последние 10–20 лет синдром раздраженной кишки стал привлекать к себе значительный научный интерес. Принятие биопсихосоциальной модели [1], применение симптомов на основе диагностических критериев (например, III Римских диагностических критериев), рост биологических и поведенческих технологий исследования [2, 3] позволили создать эффективную территорию для новых исследований СРК с перспективой для более эффективного лечения.
В настоящее время очевидно, что СРК это не одно заболевание, а четко выявляемый симптомокомплекс, который сочетает симптомы различных базовых физиологических детерминант «от кишечника к мозгу и обратно». Таким образом, одна «волшебная таблетка» в качестве лечения этого расстройства вряд ли применима: лечение должно основываться на моно- или полинаправленном фармакологическом воздействии, для целевой коррекции физиологической детерминанты, индивидуальной для каждого человека [4].
СРК — страдание, имеющее полиэтиологическую природу, характеризуется рецидивирующими болями в животе или дискомфортом наряду с нарушениями частоты или формы стула [5].
СРК имеет определенную симптоматику — «АВСD» синдрома раздраженной кишки (The ABCDs of irritable bowel syndrome):
А — боль в животе или дискомфорт, обычно в нижней части живота, но может быть без четкой локализации по всему животу (Abdominal pain or discomfort).
В — вздутие живота или ощущение распирания (Bloating or visible distention).
С — запор: затрудненная эвакуация при дефекации или редкая дефекация (Constipation: hard, difficult-to-evacuate, or infrequent stools).
D — диарея: кашицеобразный, водянистый или частый стул (Diarrhea: loose, watery, or frequent stools).
Экстракишечные симптомы, такие как усталость, головная боль, боли в спине, боль в мышцах, нарушения сна (Extra-bowel symptoms such as fatigue, headache, backache, muscle pain, and sleep disturbance).
1. Основанные на симптоматике:
- СРК с преобладанием кишечной дисфункции;
- СРК с преобладанием болевого синдрома;
- СРК с преобладанием метеоризма.
2. Основанные на наличии отягощающих факторов:
- постинфекционный СРК (ПИ-СРК);
- СРК, связанный с определенными пищевыми продуктами;
- СРК, связанный со стрессом.
В нашей статье мы хотим более подробно разобрать тип СРК, который встречается почти у каждого третьего больного, перенесшего бактериальную, вирусную или паразитарную острую желудочно-кишечную инфекцию (ОКИ) — ПИ-СРК. Впервые ПИ-СРК описали Chaudhary N. A. и Truelove S. C. [6] более 50 лет назад, после изучения 130 случаев «синдрома раздраженной толстой кишки», они выявили 26% пациентов, у которых СРК стало следствием перенесенной дизентерии.
У большинства людей, которые заболевают острой бактериальной диареей, самопроизвольное исчезновение симптомов наступает в течение < 5 дней, однако у части больных развивается неспецифическая кишечная симптоматика, которая может проявляться в течение многих лет [7]. Постинфекционный СРК развивается у 4–32% пациентов после перенесенного бактериального гастроэнтерита [8] как ответ на неспецифические инфекции, вызванные различными кишечными возбудителями, такими как, например, Campylobacter, Salmonella, диарейные штаммы Escherichia coli, Shigella, Entamoeba histolytica, Yersinia, Cryptosporidium, Legionella [9–12]. Douglas K. Rex в своем исследовании выявил, что ПИ-СРК развивается после перенесенного лямблиоза в 46% случаев, в контрольной группе в 14% [13].
ПИ-СРК диагностируется при наличии симптомов, соответствующих III Римским диагностическим критериям СРК — наличие рецидивирующей боли в животе или дискомфорта по крайней мере 3 дня в месяц за последние 3 месяца с началом симптомов не менее 6 месяцев, которые должны сочетаться с двумя или более из нижеследующих признаков: улучшение после дефекации; начало связано с изменением частоты стула; начало связано с изменением формы стула [14].
После эпизода острого инфекционного гастроэнтерита необходимо наличие двух из следующих симптомов: повышение температуры, рвота, диарея и обнаружение маркеров ОКИ в биологических средах больного [15]. Как правило, острые инфекционные симптомы — рвота и лихорадка купируются через несколько дней с разрешением инфекции, однако дискомфорт в животе, вздутие живота и диарея сохраняются [8, 9]. Ряд факторов, таких как продолжительность и тяжесть ОКИ, может увеличить риск развития ПИ-СРК [16, 17].
Ключевым фактором для развития СРК являются отклонения в работе системы мозг/кишечник. За функциональную связь компонентов системы отвечает ряд нейромедиаторов, таких как холецистокинин, вазоактивный интестинальный пептид, серотонин и др. На сегодняшний день более 60 генов исследовано на предмет их влияния на развитие СРК.
Постинфекционный СРК возникает в результате резкой ответной реакции иммунной системы на какую-либо инфекцию при последующем медленном ослаблении эффекта иммунного ответа. При этом у пациентов наблюдается слабо выраженное воспаление толстой кишки и повышенная кишечная проницаемость. Важными регуляторами иммунного ответа являются цитокины. В ряде независимых работ была выявлена связь полиморфизмов в генах IL-4, IL-6, IL-10 и фактора некроза опухоли-альфа (TNF-α), кодирующих провоспалительные интерлейкины, с развитием постинфекционного СРК. Gwee и др. [18] сообщили об увеличении экспрессии IL-1б в ректальной биопсии у пациентов с ПИ-СРК, по сравнению с теми, кто страдал инфекционным энтеритом без последующего ПИ-СРК. Wang и др. [19] также наблюдали увеличение IL-1б у пациентов с ПИ-СРК после шигеллезной инфекции по сравнению с пациентами без СРК [20]. Недавнее исследование, проведенное Villani A. и др. [21], определило три гена — TLR9, CDH1 и IL6, которые были связаны с развитием ПИ-СРК. Ген TLR9 кодирует трансмембранный рецептор, являющийся важным компонентом иммунного ответа организма. Также была обнаружена связь однонуклеотидной замены в промоторе гена CDH1, кодирующего трансмембранный гликопротеин, регулирующий межклеточную адгезию, с развитием СРК постинфекционного типа [22, 23].
У пациентов с ПИ-СРК в ряде исследований выявлено повышение уровня серотонина в энтерохромаффинных клетках (ЭК) кишечника по сравнению со здоровыми людьми. Результаты биопсии у всех пациентов были в пределах нормы с использованием обычных критериев, однако количественное исследование показало увеличение ЭК клеток (р = 0,017) по сравнению с контрольной группой (р = 0,02). Также было увеличено количество Т-лимфоцитов собственной пластинки слизистой оболочки (р = 0,026) и количество тучных клеток (р = 0,054) по сравнению с контрольной группой [24]. Увеличение на 25% в ректальной зоне числа ЭК клеток может привести к увеличению уровня серотонина и к последующей диарее [8]. У пациентов с ПИ-СРК были выявлено повышение уровня постпрандиального серотонина в плазме по сравнению с пациентами с СРК-З (запоры) и здоровыми добровольцами [25].
Воспаление слизистой оболочки кишки при ОКИ изменяет висцеральную сенсорику и часто предшествует началу симптомов в группе пациентов с ПИ-СРК. Даже легкий бессимптомный острый колит может вызывать длительную висцеральную гипералгезию при наличии дополнительных стимулов [26]. Такое «вздутие» значительно быстрее вызывало болезненную реакцию у пациентов с СРК, чем в контрольной группе [27, 28].
Риск развития ПИ-СРК коррелирует с тяжестью острой кишечной инфекции и повышается, по крайней мере, в два раза, если диарея продолжается более 1 недели, и в три раза, если диарея продолжается более 3 недель [29, 30]. Спазмы в животе и боль, потеря веса, кровавый стул увеличивают риск возникновения ПИ-СРК в четыре раза [29, 31]. Возбудители, такие как Campylobacter и Shigella, могут вызвать более серьезные повреждения слизистой и более длительные заболевания, чем Salmonella [32]. В исследовании с участием 231 пациента, которые наблюдались в течение 3 месяцев, чаще (4,2% от 119 пациентов) развивался ПИ-СРК после инфекции Campylobacter, чем после заражения сальмонеллой (2,6% из 38 пациентов), но эта разница не была значимой [17].
Sykes M. A. и соавт. [33] определили, что люди с психиатрическими преморбидными диагнозами, в частности, тревожными расстройствами, также подвергаются повышенному риску развития ПИ-СРК после ОКИ. Кроме того, депрессия, невротизации, соматизированные расстройства, стресс и негативное восприятие болезни также связаны с ПИ-СРК [34–36]. В недавнем исследовании у пациентов, у которых развился ПИ-СРК, был значительно более высокий уровень восприятия напряжения, тревоги, соматизированных расстройств и негативного отношения к заболеванию во время ОКИ, чем у тех пациентов, у которых не развивался ПИ-СРК [35]. Кроме того, Gwee и соавт. [37] установили, что пациенты с ПИ-СРК имели более высокие показатели ипохондрии. Эти наблюдения показывают психосоматические взаимодействия, которые могут вызвать симптомы ПИ-СРК и длительно поддерживать психические расстройства у этих пациентов [35]. Эта парадигма обеспечивает поддержку когнитивно-поведенческой терапии для лечения ПИ-СРК. Для объективной оценки психологической картины может помочь Шкала госпитальной тревожности и депрессии (Hospital Anxiety end Depression Seale, HADS) [38]. Мы в своей практике регулярно используем этот простой опросник из 14 пунктов, предназначенный для оценки уровня тревожности и депрессии.
Несмотря на то, что не существует гендерных различий в развитии ОКИ и иммунном ответе, риск развития ПИ-СРК выше среди женщин, чем среди мужчин [35, 39]. Женская предрасположенность к ПИ-СРК может быть обусловлена более выраженной реакцией на психологический стресс. В исследовании Gwee и др. [37] женский пол не был существенным фактором риска, когда психологические переменные контролируются в многофакторном анализе. В двух исследованиях риск развития ПИ-СРК уменьшается с увеличением возраста старше 60 лет [40]. Dunlop и соавт. [41] показали, что пожилые люди имеют меньше лимфоцитов и тучных клеток в слизистой прямой кишки, что может ослаблять воспалительные реакции и давать снижение риска ПИ-СРК.
Вероятность развития ПИ-СРК увеличивается в шесть раз после острых желудочно-кишечных инфекций при наличии следующих факторов риска развития ПИ-СРК: молодой возраст, женский пол, диарея > 7 дней, наличие крови в кале, боль в животе, потеря веса, по крайней мере, десять фунтов (примерно 4,5 кг), тревожное или депрессивное расстройство, ипохондрия, предшествующие неблагоприятные жизненные события [42].
Диагноз ПИ-СРК является диагнозом, который может быть поставлен после тщательного обследования больного, позволяющего исключить у пациента органические заболевания ЖКТ. Решающее значение в обследовании больных с ПИ-СРК имеют данные ирригоскопии, компьютерной колоноскопии, дуоденоскопии, сигмоскопии или эндоскопической колоноскопии для исключения воспалительных заболеваний кишечника, целиакии, паразитозов и других заболеваний кишечника (табл.). Показано обследование кала для определения количества лейкоцитов, скрытой крови, паразитов. Выявление дивертикулеза кишечника не противоречит диагнозу ПИ-СРК. У некоторых больных с целиакией и спру также выявляются симптомы ПИ-СРК. У больных с ПИ-СРК с HLA-DQ2 и интестинальными антителами к глиадину и другим пищевым протеинам после ограничения глютена частота дефекаций и уровень кишечных Ig уменьшаются.
Лечение ПИ-СРК, как правило, симптоматически направленное и включает в себя диетические рекомендации, психотерапию и средства, предназначенные для лечения СРК с диареей (СРК-Д). Эмпатия и поддержка доктора имеют решающее значение для пациента. Врач должен подчеркнуть, что ПИ-СРК не является опасным для жизни расстройством, и должен успокоить пациента, объяснить, что его симптомы не являются мнимыми и связаны с различными факторами. Диетические рекомендации направлены на исключение продуктов, провоцирующих диарею и метеоризм, пища должна быть химически и термически щадящая с хорошей кулинарной обработкой. Психотерапевтические мероприятия направлены на устранение напряжения, тревоги, депрессии, ипохондрии и включают в себя различные методики и/или психотропную коррекцию. Разумно назначать психотропные препараты, которые имеют побочным эффектом запоры и в данной ситуации работают как анксиолитики или антидепрессанты, при этом уменьшая или устраняя диарею. К таким препаратам относятся сульпирид, амитриптилин, антидепрессанты с точкой приложения 5-НТ1— или 5-НТ3-рецепторов, антигистаминные и ГАМКергические анксиолитики.
Антидиарейные средства, такие как лоперамид, могут быть эффективными в снижении частоты диареи. Лоперамид тормозит перистальтику и секрецию жидкости, что приводит к увеличению транзитного времени желудочно-кишечного тракта, повышает поглощение жидкости и электролитов в желудочно-кишечном тракте. Тем не менее, лоперамид не уменьшает боли в животе, которые связаны с ПИ-СРК [44]. Общие побочные реакции на лоперамид включают судороги и тошноту. Также необходимо исключить синдром избыточного бактериального роста (СИБР) в тонкой кишке, при котором прием лоперамида может усилить интоксикацию.
Достаточно часто ПИ-СРК бывает ассоциирован с СИБР, особенно после курсов специфической терапии ОКИ. У таких пациентов еще более выражены синдромы мальабсорбции, мальдигестии, нарушена деконъюгация желчных кислот, беспокоят метеоризм, диарея и боль в животе. Исключить или подтвердить диагноз СИБР помогает дыхательный водородный тест с лактулозой. При сочетании ПИ-СРК и СИБР показано применение антибиотиков [45], пребиотиков и пробиотиков [38]. Препаратом выбора для деконтаминации тонкой кишки во многих исследованиях и рекомендациях стал рифаксимин, который показал хорошие результаты при лечении СРК. В рандомизированном плацебо-контролируемом исследовании 124 пациентов проведен 10-дневный курс рифаксимина 400 мг 3 раза в день или плацебо, рифаксимин статистически значимо уменьшал вздутие живота и флатуленцию [46]. Эти результаты были подтверждены в двойном слепом, плацебо-контролируемом исследовании с участием 87 пациентов с СРК в 2006 году. По окончании лечения большинство пациентов в группе рифаксимина отмечали значительное уменьшение симптомов СРК (37,7% против 23,4%) (p < 0,05) и стойкий клинический ответ (37,2% против 15,9%) (р < 0,05) [47].
Ведущий симптом ПИ-СРК — боль, вызванная спазмом, в основе которого лежит непроизвольное сокращение гладких мышц кишечника, не сопровождающееся их немедленным расслаблением. Главные механизмы развития абдоминальной боли обусловлены нарушением моторики кишечника и висцеральной гиперчувствительностью. В национальных практических руководствах по СРК (Guideline IBS) разных стран рекомендуются основные спазмолитики различных групп: отилония бромид, тримебутин, циметропия бромид, гиосцина бутилбромид, пинаверия бромид, алверина цитрат, мебеверин, в том числе и масло перечной мяты. Почти все они показали значительное преимущество по сравнению с плацебо [48]. В зависимости от основного механизма воздействия на этапы сокращения мышечного волокна выделяют несколько групп мышечных релаксантов.
Антихолинергические средства (атропин, платифилин, гиосцина бутилбромид) снижают концентрацию интрацеллюлярных ионов кальция, что приводит к мышечной релаксации. Важно отметить, что степень релаксации находится в прямой зависимости от предшествующего тонуса парасимпатической нервной системы.
Блокаторы фосфодиэстеразы — миотропные спазмолитики (папаверин, дротаверин) способствуют накоплению в клетке цАМФ и уменьшению концентрации ионов кальция, что тормозит соединение актина с миозином. Данные препараты используются кратковременно (от однократного приема до недели) для купирования спазма, но не для курсового лечения, направленного на купирование и профилактику рецидива заболевания.
Определенное значение в регуляции моторной функции органов ЖКТ отводится эндогенным опиатам. В настоящее время в лечении больных СРК используется агонист опиатных рецепторов — тримебутин — регулятор моторики ЖКТ. В рандомизированных плацебо-контролируемых исследованиях по СРК Quartero A. O. и соавт. (2005) и Ford A. C. и соавт. (2008) тримебутин не показал значительного преимущества и статистически значимо не отличался от плацебо [49, 50].
Пинаверия бромид (Дицетел®), основным действующим веществом которого является пинаверия бромид, представляет собой спазмолитик миотропного действия — антагонист кальция для лечения нарушений перистальтики кишечника [51]. Он избирательно блокирует потенциалзависимые кальциевые каналы гладкой мускулатуры кишечника и препятствует избыточному поступлению кальция внутрь клетки. В отличие от других антагонистов кальция, Дицетел® проявляет одинаковое сродство к каналам в доступном и инактивированном состоянии, что обусловливает его высокую эффективность и отсутствие привыкания [52]. Сбалансированная работа гладкомышечного аппарата желудочно-кишечного тракта зависит от концентрации кальция в цитоплазме миоцита и его перемещений через клеточную мембрану. Ионы кальция играют роль не только в связке «возбуждение-сокращение», но и в связке «возбуждение-расслабление». Кальциевые каналы L-типа гладкомышечных клеток ЖКТ активируются двумя путями:
- Первый, наиболее полно изученный, характеризуется деполяризацией клеточной мембраны посредством воздействия нервного импульса, с последующим сокращением гладкомышечной клетки.
- Второй способ включает активацию кальциевого канала пищеварительными гормонами и медиаторами, такими как холецистокинин, гастрин или субстанция P. Связываясь со специфическими рецепторами, они активируют рецептор-управляемые Са2+-каналы, что вызывает деполяризацию клеточной мембраны и приводит к открытию потенциал-зависимых кальциевых каналов. В случае если кальциевые каналы заблокированы молекулами пинаверия бромида, действие вышеуказанных пищеварительных гормонов и медиаторов не может быть реализовано.
Таким образом, пинаверия бромид ингибирует не только гипермоторику кишечника, но и путь, вовлеченный в висцеральную гиперчувствительность, — второй признак синдрома раздраженного толстого кишечника. Кроме того, в мембранах гладкомышечных клеток кишечника человека недавно были открыты кальциевые каналы, чувствительные к механическим воздействиям. Существование такого типа кальциевых каналов может изменить представление о желудочно-кишечной гладкой мускулатуре как о «сугубо двигательном органе», обладающем как двигательной, так и сенсорной функцией. Об эффективности применения Дицетела® у больных СРК всех типов свидетельствует большое количество исследований как в нашей стране, так и за рубежом [53–56]. Большинство исследователей показывают хорошие и очень хорошие результаты по полному купированию и уменьшению интенсивности боли при СРК на фоне приема Дицетела® в качестве монотерапии в стандартной дозировке (на уровне более 60%).
Обзор 22 рандомизированных контролируемых исследований (n = 1778), в которых проводилось сравнение 12 различных спазмолитиков (в том числе пинаверия бромид, тримебутин и дицикломин), показал статистически значимый эффект терапии. Уменьшение болевого синдрома имело место у 39% пациентов, получающих лечение, и у 56% пациентов, получающих плацебо. При этом пинаверия бромид показал статистически значимый эффект терапии, в отличие от тримебутина. Болевой синдром сохранился у 28% пациентов, получающих лечение, и у 61% пациентов, получающих плацебо [49, 50].
Дицетел® в начальном периоде заболевания при выраженном болевом синдроме (3–6 дней) назначается по 100 мг 2–3 раза в сутки во время еды. Суточная доза Дицетела® (таблетки, покрытые пленочной оболочкой, 100 мг) — по 1 таблетке 2 раза в сутки, утром и вечером во время еды. Если необходимо, суточная доза может быть увеличена до 3 таблеток в сутки. После стихания обострения поддерживающей дозировкой пинаверия бромида является стандартная доза — 50 мг 3–4 раза в сутки, назначаемая на курс от 2 до 6 недель и более. Действуя селективно на кишечник, Дицетел® не имеет побочных антихолинергических эффектов, поэтому его можно без опасений назначать пациентам с глаукомой и гипертрофией предстательной железы.
В своей клинической практике мы достаточно часто встречаемся с СРК, в том числе и с ПИ-СРК. Особенности течения ПИ-СРК заключаются в более выраженной и длительной диарее и стойком болевом синдроме.
Интересные клинические случаи из нашей практики
Пациент М., 35 лет. В декабре 2009 года перенес тяжелый стресс (смерть матери от онкологического заболевания), через несколько дней началась диарея до 5–7 раз в сутки, которая прогрессировала, самостоятельные попытки купировать симптоматику были тщетны. В январе 2010 года обратился к инфекционисту, при обследовании были выявлены антитела к иерсиниозу, проведен курс лечения антибиотиками. Диарея сохранялась. В феврале 2010 года при повторном обследовании титр антител к иерсинизу сохранялся на прежнем уровне, курс антибиотикотерапии был повторен. После второго курса лечения дирейный синдром не купировался. За время лечения потеря веса более 10 килограмм, резко снизилась трудоспособность, наблюдались выраженная слабость, ангедония, канцерофобия, бессонница. С марта по апрель 2010 года был на приеме у нескольких гастроэнтерологов, обследование — клинические и биохимические анализы крови, ирригоскопия, колоноскопия, копроовоскопия — без патологии, обычное лечение диареи (лоперамид, смекта) было малоэффективным. В мае 2010 года назначен курс лечения с учетом основных симптомов ПИ-СРК: Дицетел® по 100 мг 3 раза в сутки в течение месяца, Просульпин 50 мг 3 раза в сутки в течение месяца. Назначен дыхательный водородный тест с лактулозой, в результате которого выявлена высокая бактериальная контаминация тонкой кишки. К лечению добавлен Альфа Нормикс 400 мг 3 раза в сутки — курс 6 дней, затем Линекс по 2 капсулы 3 раза в сутки — курс 14 дней и Дюфалак® по 5 мл до 3 месяцев. Через месяц лечения отмечает значительное улучшение, стул не чаще 1–2 раз утром после завтрака, остается умеренная тревожно-депрессивная симптоматика, страх возврата диареи. Дицетел® рекомендован для приема по потребности при болях в животе, вместо Просульпина назначен Тразодон по 150 мг в сутки до 6 месяцев. В декабре 2010 года — следующий визит к гастроэнтерологу — жалоб не предъявляет, вес восстановился, занимается спортом, вернулся к обычной профессиональной деятельности.
Пациентка П., 86 лет. Направлена инфекционистом в апреле 2012 года с выраженным абдоминальным болевым синдромом, диареей, страхом приема пищи, которая усиливает боль в животе. В анамнезе месяц назад перенесла ОКИ в сочетании с лямблиозом, лечилась антибиотиками, нитрофуранами, похудела на 7–8 кг. Обследования — клинические и биохимические анализы крови, УЗИ органов брюшной полости, ФГДС, колоноскопия — в пределах возрастной нормы. При водородном дыхательном тесте с лактулозой выявлен СИБР. Назначено лечение: Дицетел® по 100 мг 3 раза в сутки в течение месяца, Альфа Нормикс 400 мг 2 раза в сутки в течение 6 дней, затем РиоФлора Баланс по 2 капсулы 2 раза в сутки в течение 14 недель. Через месяц на приеме гастроэнтеролога — значительное улучшение самочувствия, боль в животе возникает значительно реже, стул не чаще 2 раз в сутки, остается страх приема пищи, нарушенный сон. Рекомендован прием Дицетела® по 50–100 мг при болях в животе по потребности, флувоксамин по 50 мг на ночь в течение полугода. В июне 2012 года отмечает значительное улучшение самочувствия, прибавку в весе, стул нормализовался, расширила рацион употребляемых продуктов, продолжает прием флувоксамина.
Заключение. Лечение ПИ-СРК должно иметь четкие и реалистичные цели, к которым необходимо стремиться как врачу, так и пациенту. Согласованная тактика лечения должна включать в себя мероприятия на уменьшение симптомов (или исключение) и улучшение качества жизни пациентов. Большинство пациентов нуждаются в коррекции СИБР путем деконтаминации тонкой кишки с помощью современных энтеросептиков. Части пациентов с течением ПИ-СРК средней степени тяжести и тяжелым часто необходима рациональная психотерапия, назначение препаратов разных фармакологических групп — спазмолитиков, пробиотиков, пребиотиков, антибиотиков, антидирейных препаратов, антидепрессантов и некоторых других, при необходимости — психотерапия. Разумно использовать различные схемы этих препаратов как для лечения симптомов обострения, так и с профилактической целью для удлинения ремиссии и улучшения качества жизни пациентов с постинфекционным синдромом раздраженной кишки.
Литература
- Drossman D. A. Presidential address: gastrointestinal illness and the biopsychosocial model // Psychosom Med. 1998. 60. Р. 258–67.
- Drossman D. A. The functional gastrointestinal disorders and the Rome III process. In: Drossman D. A., Corazziari E., Delvaux M., Spiller R., Talley N. J., Thompson W. G. et al. Rome III: The Functional Gastrointestinal Disorders. 3 rd ed. McLean, VA: Degnon Associates. 2006. Р. 1–30.
- Drossman D. A. The functional gastrointestinal disorders and the Rome III process // Gastroenterology. 2006. 130. Р. 1377–1390.
- Drossman D. A. Treatment for Bacterial Overgrowth in the Irritable Bowel Syndrome // Comment on: Ann Intern Med. 2006. Oct 17. 145 (8). Р. 557–563.
- Longstreth G. F., Thompson W. G., Chey W. D. et al. Functional bowel disorders // Gastroenterology. 2006. 130. Р. 1480–1491.
- Chaudhary N. A., Truelove S. C. The irritable colon syndrome: a study of the clinical features, predisposing causes, and prognosis in 130 cases // Q J Med. 1962. 31. Р. 307–322.
- Neal K. R., Barker L., Spiller R. C. Prognosis in post-infective irritable bowel syndrome: a six year follow up study // Gut. 2002. 51. Р. 410–413.
- Spiller R. C., Campbell E. Post-infectious irritable bowel syndrome // Curr Opin Gastroenterol. 2006. 22. Р. 13–17.
- Spiller R. C., Jenkins D., Thornley J. P. et al. Increased rectal mucosal enteroendocrine cells, T lymphocytes and increased gut permeability following acute Campylobacter enteritis and in post-dysenteric irritable bowel syndrome // Gut. 2000. 47. Р. 804–811.
- Gwee K. A., Collins S. M., Read N. W. Increased rectal mucosal expression of interleukin 1β in recently acquired postinfectious irritable bowel syndrome // Gut. 2003. 52. Р. 523–526.
- Wang L. H., Fang X. C., Pan G. Z. Bacillary dysentery as a causative factor of irritable bowel syndrome and its pathogenesis // Gut. 2004. 53. Р. 1096–1101.
- Triantafillidis J. K., Peros G. Post-infectious Irritable bowel syndrome // Annals of Gastroenterology. 2007. 20 (4). Р. 243–245.
- Douglas K. Rex. Add Parasites to the Causes of Postinfectious Irritable Bowel Syndrome // Gut. 2012. Feb. 61. Р. 214.
- Longstreth G. F., Thompson W. G., Chey W. D. et al. Functional bowel disorders // Gastroenterology. 2006. 130. Р. 1480–1491.
- Dunlop S. P., Jenkins D., Spiller R. C. Distinctive histological patterns of chronic inflammatory cells in rectal biopsies of patients with different clinical subtypes of IBS // Gastroenterology. 2002. 122 (Suppl 1). Р. 60.
- Neal K. R., Hebden J., Spiller R. Prevalence of gastrointestinal symptoms six months after bacterial gastroenteritis and risk factors for development of the irritable bowel syndrome: postal survey of patients // BMJ. 1997. 314. Р. 779–782.
- Borgaonkar M. R., Ford D. C., Marshall J. K. et al. The incidence of irritable bowel syndrome among community subjects with previous acute enteric infection // Dig Dis Sci. 2006. 51. Р. 1026–1032.
- Gwee K. A., Collins S. M., Read N. W. et al. Increased rectal mucosal expression of interleukin 1 beta in recently acquired post-infectious irritable bowel syndrome // Gut. 2003. 52. Р. 523–526.
- Marshall J. K., Thabane M., Garg A. X. et al. Intestinal permeability in patients with irritable bowel syndrome after a waterborne outbreak of acute gastroenteritis in Walkerton, Ontario // Aliment Pharmacol Ther. 2004. 20. Р. 1317–1322.
- Wang L. H., Fang X. C., Pan G. Z. Bacillary dysentery as a causative factor of irritable bowel syndrome and its pathogenesis // Gut. 2004. 53. Р. 1096–1101.
- Villani A., Lemire M., Thabane M. Genetic risk factors for post-infectious IBS in the E. coli 0157: H7 outbreak in Walkerton (Canada) in 2000 // Gastroenterology. 2008. 134. A122.
- Zanini B. Norovirus gastroenteritis may lead to post-infectious IBS // Am J Gastroenterol. 2012. doi:10. Р. 1038.
- Van der Veek P. P., Van den Berg M., de Kroon Y. E. Role of tumor necrosis factor-alpha and interleukin-10 gene polymorphisms in irritable bowel syndrome // Am J Gastroenterol. 2005. 100. Р. 2510–2516.
- Dunlop S. P., Jenkins D., Spiller R. C. Distinctive clinical, psychological, and histological features of postinfective irritable bowel syndrome // Am J Gastroenterol. 2003. 98. Р. 1578–1583.
- Dunlop S. P., Coleman N. S., Blackshaw E. et al. Abnormalities of 5-hydroxytryptamine metabolism in irritable bowel syndrome // Clin Gastroenterol Hepatol. 2005. 3. Р. 349–357.
- Adam B Liebregts T., Gschossmann J. M. et al. Severity of mucosal inflammation as a predictor for alterations of visceral sensory function in a rat model // Pain. 2006. 123. Р. 179–186.
- Rogers J., Henry M. M., Misiewicz J. J. Increased segmental activity and intraluminal pressures in the sigmoid colon of patients with the irritable bowel syndrome // Gut. 1989. 30. Р. 634–641.
- Ritchie J. Pain from distension of the pelvic colon by inflating a balloon in the irritable colon syndrome // Gut. 1973. 14. Р. 125–132.
- Marshall J. K., Thabane M., Garg A. X. et al. Incidence and epidemiology of irritable bowel syndrome after a large waterborne outbreak of bacterial dysentery // Gastroenterology. 2006. 131. Р. 445–450.
- Neal K. R., Hebden J., Spiller R. Prevalence of gastrointestinal symptoms six months after bacterial gastroenteritis and risk factors for development of the irritable bowel syndrome: postal survey of patients // BMJ. 1997. 314. Р. 779–782.
- Wang L. H., Fang X. C., Pan G. Z. Bacillary dysentery as a causative factor of irritable bowel syndrome and its pathogenesis // Gut. 2004. 53. Р. 1096–1101.
- Connor B. A. Sequelae of traveler’s diarrhea: focus on postinfectious irritable bowel syndrome // Clin Infect Dis. 2005. 41 (suppl 8). S. 577-S586.
- Sykes M. A., Blanchard E. B., Lackner J. et al. Psychopathology in irritable bowel syndrome: support for a psychophysiological model // J Behav Med. 2003. 26. Р. 361–372.
- Parry S. D., Stansfield R., Jelley D. et al. Does bacterial gastroenteritis predispose people to functional gastrointestinal disorders? A prospective, community-based, case-control study // Am J Gastroenterol. 2003. 98. Р. 1970–1975.
- Spence M. J., Moss-Morris R. The cognitive behavioural model of irritable bowel syndrome: a prospective investigation of patients with gastroenteritis // Gut. 2007. 56. Р. 1066–1071.
- Dunlop S. P., Jenkins D., Neal K. R., Spiller R. C. Relative importance of enterochromaffin cell hyperplasia, anxiety, and depression in postinfectious IBS // Gastroenterology. 2003. 125. Р. 1651–1659.
- Gwee K. A., Leong Y. L., Graham C. et al. The role of psychological and biological factors in postinfective gut dysfunction // Gut. 1999. 44. Р. 400–406.
- Quigley E., Fried M., Gwee K. A. at al. Практические рекомендации Всемирной гастроэнтнрологической организации. Синдром раздраженного кишечника: глобальные перспективы. 20 апреля 2009. http://www.worldgastroenterology.
- Tuteja A. K., Talley N. J., Gelman S. S. et al. Development of functional diarrhea, constipation, irritable bowel syndrome, and dyspepsia during and after traveling outside the USA // Dig Dis Sci. 2008. 53. Р. 271–276.
- Neal K. R., Hebden J., Spiller R. Prevalence of gastrointestinal symptoms six months after bacterial gastroenteritis and risk factors for development of the irritable bowel syndrome: postal survey of patients // BMJ. 1997; 314: 779–782.
- Dunlop S. P., Jenkins D., Spiller R. C. Age-related decline in rectal mucosal lymphocytes and mast cells // Eur J Gastroenterol Hepatol. 2004. 16. Р. 1011–1015.
- Thabane M., Kottachchi D. T., Marshall J. K. Systematic review and meta-analysis: The incidence and prognosis of post-infectious irritable bowel syndrome // Aliment Pharmacol Ther. 2007. Aug. 15. 26 (4). Р. 535–544.
- Herbert L. DuPont. Postinfectious Irritable Bowel Syndrome: Clinical Aspects, Pathophysiology, and Treatment // Practical Gastroenterology. 2007. Volume XXXI. Issue 9. Р. 18–24.
- Baker D. E. Loperamide: a pharmacological review // Rev Gastroenterol Disord. 2007. 7 (suppl 3). S. 11-S18.
- Viera J. A., Hoag S., Shaugnessy J. Management of Irritable Bowel Syndrome // Am Fam Physician. 2002. Nov. 15. 66 (10). Р. 1867–1875.
- Sharara A. I., Aoun E., Abdul-Baki H. et al. A randomized double-blind placebo-controlled trial of rifaximin in patients with abdominal bloating and flatulence // Am J Gastroenterol. 2006. 101. Р. 326–333.
- Pimentel M., Park S., Mirocha J. et al. The effect of a nonabsorbed oral antibiotic (rifaximin) on the symptoms of the irritable bowel syndrome: a randomized trial // Ann Intern Med. 2006 145. Р. 557–563.
- National Collaborating Centre for Nursing and Supportive Care. Irritable bowel syndrome in adults. Diagnosis and management of irritable bowel syndrome in primary care. London (UK): National Institute for Health and Clinical Excellence (Clinical guideline; no. 61). 2008, Feb. 881 p.
- Ford A. C., Talley N. J., Spiegel M. R. et al. Effect of fibre, antispasmodics, and peppermint oil in the treatment of irritable bowel syndrome: systematic review and meta-analysis // BMJ. 2008. 337. 2313.
- Quartero A. O., Meineche-Schmidt V., Muris J. et al. Bulking agents, antispasmodic and antidepressant medication for the treatment of irritable bowel syndrome // Cochrane Database of Systematic Reviews. 2005 (2). CD003460.
- Wesdorp I. The central role of Ca++ as mediator of gastrointestinal motility. In: Calcium antagonism & Gastrointestinal motility // Experta Medica. 1989. P. 20–27.
- McCallum R. W. The role of calcium and calcium antagonism in motility disorders of the gastrointestinal tract. In: Calcium antagonism & Gastrointestinal motility // Experta Medica. 1989. P. 28–31.
- Guslandi М. The clinical pharmacological profile of pinaverium bromide // Minerva Med. 1994. Apr. 85 (4). Р. 179–85.
- Wittmann T., Feher A., Rosztoczy A., Janosi J. Effectiveness of pinaverium bromide therapy on colonic motility disorders in irritable bowel syndrome // Orv Hetil. 1999. Feb 28. 140 (9). Р. 469–73.
- Awad R. A., Cordova V. H., Dibildox M. et al. Reduction of post-prandial motility by pinaverium bromide a calcium channel blocker acting selectively on the gastrointestinal tract in patients with irritable bowel syndrome // Acta Gastroenterol Latinoam. 1997. 27 (4). Р. 247–51.
- Christen M. O. Action of pinaverium bromide, a calcium-antagonist, on gastrointestinal motility disorders // General Pharmacology: The Vascular System. 1990 V. 21. Issue 6. P. 821–825.
А. А. Самсонов*, доктор медицинских наук, профессор
Е. Ю. Плотникова**, доктор медицинских наук, профессор
М. В. Борщ***
*ГБОУ ВПО МГМСУ Минздравсоцразвития России, Москва
**ГБОУ ВПО КемГМА Минздравсоцразвития России, Кемерово
***МБЛПУ ГКБ № 1, Новокузнецк
Контактная информация об авторах для переписки: eka-pl@rambler.ru









![Дифференциальный диагноз с ПИ-СРК [42]](https://www.lvrach.ru/img/default.webp)